Häufigere Prostatakrebserkrankungen in einzelnen Familien beruhen nicht unbedingt auf einer vererbbaren familiären Prädisposition. Vielmehr gibt es im familiären Umfeld häufig gemeinsame, nicht genetisch bedingte Einflüsse. Hierzu gehören u. a. bestimmte Verhaltensweisen und Ernährungsgewohnheiten, die manchmal über viele Generationen „vererbt“ werden und das Erkrankungsrisiko negativ beeinflussen.
Grundsätzlich gibt es verschiedene Ansatzpunkte, über die die Ernährung die verschiedenen Phasen der Krebsentwicklung beeinflusst. So können Enzymsysteme zur Bildung von Kanzerogenen beitragen und auf diesem Wege Genmutationen verursachen; Viren in den Lebensmitteln, Benzpyrene und polyzyklische aromatische Kohlenwasserstoffe können Mutationen verursachen und so zur Krebsentstehung beitragen.
Lesen Sie jetzt den kompletten Ratgeber: Prostatakrebs vermeiden jetzt bestellen
Eine direkte Einwirkung von Nahrungsbestandteilen auf der molekularen Ebene (Tumoriniation) ist jedoch wesentlich seltener als Einwirkungen auf die zweite Phase der Krebsentwicklung, in der Anreize zum Wachstum der Krebszellen und Krebsvorstufen gegeben werden (Tumorpromotion) (Abbildung).
Je nach Ernährungsweise kommt es zu einer Begünstigung oder Hemmung des Krebswachstums. Entgegen der volkstümlichen Vorstellung und unzähliger Berichte in der Laienpresse wissen wir allerdings viel weniger über krebshemmende als krebsfördernde Einflüsse der Ernährung.
Sind Zusammenhänge von Ernährung und Prostatakrebserkrankungen eindeutig?
Zusammenhänge von Ernährung und Prostatakrebserkrankungen sind zwar wahrscheinlich, jedoch objektiv schwer nachzuweisen. Einer der Grund hierfür ist, dass sich der Einfluss der „Ernährung“ nur schwer von anderen Krebsrisiken trennen lässt. Dass z. B. Prostatakrebs bei Adventisten seltener ist als in der Allgemeinbevölkerung liegt nicht nur daran, dass diese sich vegetarisch ernähren, sondern im Allgemeinen auch schlanker und körperlich aktiv sind, auf Alkohol verzichten und insgesamt gesundheitsbewusster leben.
Um an Prostatakrebs zu erkranken, bedarf es verschiedener Einflüsse zu unterschiedlichen Zeitpunkten. Prostatakrebs entsteht nicht von heute auf morgen. Von der Entstehung erster Krebszellen bis zum Ausbruch der Krankheit dauert es viele Jahre, in denen sich das Ernährungsverhalten häufig ändert.
Bis heute konnte in keiner einzigen Studie ein eindeutiger Nachweis für die Beeinflussung des Krebsrisikos durch bestimmte Ernährungsweisen und erst recht nicht durch einzelne Nahrungsbestandteile erbracht werden. Wenn überhaupt, zeichnen sich in den Studienergebnissen lediglich statistisch nicht signifikante Tendenzen bei der Nahrungsmittelauswahl, der Nahrungszubereitung und dem Ernährungsverhalten ab. Diese sollten aber dennoch ernst genommen werden.
Es gibt unzählige Studien, die sich mit dem Einfluss der Ernährung auf das Erkrankungsrisiko befasst haben und Zusammenhänge herstellen, obwohl epidemiologische Studien keine kausalen Gemeinsamkeiten sehen, sondern lediglich Assoziationen und Risikofaktoren identifizieren können. Die Evidenz ist sehr häufig aus mehreren Gründen nicht überzeugend.
Um die Aussagefähigkeit der Studien zu beurteilen, müssen die unten aufgeführten Aspekte beachtet werden.
Methodische Aspekte, die in Studien zur Krebsvorbeugung häufig nicht beachtet werden
- Wo wurden die Studien durchgeführt? Manche Studienergebnisse stammen aus Beobachtungen in außereuropäischen Regionen, teilweise bei anderen Ethnien und bei anderen Umwelteinflüssen. (Obwohl die Ernährungsgewohnheiten häufig nicht mit unsrigen vergleichbar und auf Mitteleuropa übertragbar sind, werden sie häufig irrtümlich als Argument für oder gegen einen Einfluss der Ernährung zitiert).
- Um welche Art von Prostatakrebs handelt es sich? Hinter dem Begriff Prostatakrebs verbergen sich sowohl zufällig erkannte und harmlose Prostatakrebserkrankungen als auch behandlungsbedürftige Erkrankungen in den unterschiedlichsten Ausbreitungsstadien. (Es gibt Hinweise dafür, dass je nach Gewebetyp und je nach Ausbreitungsgrad unterschiedliche Einflussfaktoren auf die Krebsentwicklung wirksam sein können). Studien, die keine nähere Differenzierung der Tumore vornehmen, haben nur eine geri8nge Aussagekraft.
- Um was für ein „Studiendesign“ handelt es sich? Wichtig ist zu wissen, ob die Schlussfolgerungen auf Befragungen Betroffener zu ihrem Ernährungsverhalten in der Vergangenheit basierten oder ob es sich um eine prospektiv angelegte Verlaufsstudie handelte, während der das Ernährungsverhalten und die Vorkommnisse dokumentiert wurden? Die meisten Schlussfolgerungen und Empfehlungen basieren auf Befragungen von Betroffenen. Deren Angaben sind erfahrungsgemäß sehr unzuverlässig, subjektiv gefärbt und beruhen auf Angaben in einem begrenzten Zeitraum, meist sogar nur in den letzten Jahren vor der Erkrankung. Dem steht entgegen, dass viele Jahre, ja Jahrzehnte bis zur Entwicklung von Krebsvorstufen und deren bösartige Entartung notwendig sind. Weitere Jahre braucht es, bis latente Frühkarzinome sich schließlich zu einer manifesten Krebserkrankung entwickeln, die sich auch auf andere Organe ausdehnt. Risikofaktoren können über das gesamte Leben eine Rolle spielen bzw. Mutationen verursachen und/oder das Wachstum von Tumorzellen beschleunigen. (Langjährige Ernährungsgewohnheiten haben eine größere Bedeutung als kurzfristige „Diätsünden“!).
- War die Anzahl der untersuchten Personen repräsentativ? Die Anzahl der untersuchten Probanden und analysierten Verläufe sowie Beobachtungsjahre ist häufig zu gering. Häufig werden keine altersangepassten Analysen vorgenommen, obwohl bei jungen Menschen das Gewebe anders auf Schadstoffe reagiert als bei älteren Menschen und die Fähigkeit zur Reparatur und Elimination von Krebsgenen sich bei jungen Menschen wahrscheinlich von denen bei älteren Menschen unterscheidet. Studien, in denen der überprüfte Personenkreis klein und darüber hinaus selektiv und nicht repräsentativ ist, sind wenig aussagekräftig.
- Handelt es sich tatsächlich um Untersuchungen bei Menschen? Häufig werden Erfahrungen aus Tierversuchen und Studien mit Zellkulturen auf Menschen übertragen, (was nicht statthaft ist!).
- Wurde zwischen Einflüssen auf die Krebsentstehung und Einflüssen auf den Krankheitsverlauf unterschieden? In einigen Studien werden Einflüsse auf die Krebsentstehung mit Einflüssen auf den Tumorverlauf vermischt (obwohl gesundes Gewebe ganz anders als krankes Gewebe auf Einflüsse reagiert und sich die Empfindlichkeit für Schadstoffe im Verlauf einer Krebserkrankung ändert).
- Wurden die unterschiedlichen Ergebnisse der Vergleichsgruppen in Relativprozent oder in Absolutzahlen angegeben? In einigen Studien werden Vergleiche und Ergebnisse in Prozent und in anderen in absoluten Zahlen ausgedrückt. (Angaben in Relativprozenten vermitteln im Gegensatz zu Absolutzahlen einen übertriebenen Eindruck).
- Handelt es sich um eine einzelne Studie oder um die Zusammenfassung mehrerer Studien? Viele Empfehlungen zur Vorbeugung gegen Darmkrebs sind in den letzten Jahren in kontrollierten Studien überprüft und in so genannten systematischen Übersichten (Metastudien) zusammengefasst worden. (Schlussfolgerungen und Empfehlungen auf dem Boden von Metastudien sind zuverlässiger als Schlussfolgerungen einzelner Studien!).
- Handelt es sich um eine retrospektive oder um eine prospektive Studie? Ergebnisse und Schlussfolgerungen von retrospektiven Studien müssen kritisch gewertet werden. (Prospektive Studien sind aussagefähiger. Sie sind jedoch weitaus in der Minderzahl!).
Den höchsten Evidenzgrad bzw. die größte Relevanz haben „Interventionsstudien“. In ihnen wird der Einfluss einer bestimmten Maßnahme oder eines bestimmten Wirkstoffes – am besten randomisiert, placebokontrolliert und doppelblind – in einer definierten Gruppe untersucht.
Solche Interventionsstudien gibt es zur Frage nach der Beeinflussung des Prostatakrebsrisikos durch die Ernährung nicht. Sie wird es voraussichtlich auch in der Zukunft nicht geben. Ein Grund neben den ethischen Bedenken hierfür ist die notwendige Dauer einer solchen Interventionsstudie. Sie müsste Jahrzehnte dauern, um relevante Ergebnisse für den Endpunkt „Verhinderung einer Krebserkrankung“ zu erzielen. Es ist nicht zu erwarten, dass es von einer bestimmten Ernährungsweise zu kurzfristigen Auswirkungen auf das Krebswachstum kommt.
Gibt es eine Klassifikation zur Evidenz von Empfehlungen in Studien?
Die Deutsche Krebsgesellschaft und verschiedene Fachgesellschaften, die sich in Deutschland
mit der Ermittlung von Krebsrisiken und den Empfehlungen zur Krebsreduzierung befassen, haben eine Klassifikation erarbeitet, die eine Wertung der Aussagekraft von Studien und Empfehlungen ermöglicht.
Klassifikation der Empfehlungsgrade
| A: | Konsistente Studien mit Evidenzgrad 1 vorhanden |
| B: | Konsistente Studien mit Evidenzgrad 2 oder 3 bzw. Extrapolationen von Studien mit Evidenzgrad 1 |
| C: | Studien mit Evidenzgrad 4 oder Extrapolationen von Studien mit Evidenzgrad 2 oder 3 |
| D: | Expertenmeinung oder inkonsistente bzw. nicht schlüssige Studien jedes Evidenzgrades |
Welche Bedeutung hat die EPIC Studie?
Zu der Frage möglicher Zusammenhänge von Krebs und Ernährung sind in den letzten Jahren einige quantitativ und qualitativ sehr aufwändige prospektive kontrollierte Studien durchgeführt worden, die zu erheblichen Korrekturen von Vorstellungen und Schlussfolgerungen älterer Studien führten.
Eine dieser Studien ist die EPIC Studie (EPIC = European Prospective Investigation into Cancer and Nutrition) (Van Gils et al 2005, und Riboli 2001, Bofetta et al 2010), die seit 1989 bei mehr als 500.000 Gesunden in verschiedenen Ländern Europas durchgeführt wird. Sie enthält wesentliche Daten des Lebensstils, darunter Detaildaten zum Körpergewicht, zur körperlichen Aktivität, zur Ernährung, zum Tabakstoff -/Nikotinabusus und Alkoholkonsum und der im Studienverlauf auftretenden Erkrankungen (http: //epic.iarc.fr).
Generell zeichnet sich in der 2014 immer noch nicht abgeschlossenen Studie ab, dass kaum eine der früheren Behauptungen zur Ernährung zuverlässig wissenschaftlich untermauert war. Sie ergab, dass einige Ernährungsfaktoren in ihrer Wirkung überschätzt, andere unterschätzt, manche auch falsch eingeschätzt wurden. Sie misst insgesamt den Einflüssen der Ernährung auf die Prostatakrebsentstehung eine geringere Bedeutung bei als frühere Studien, bestätigt aber andererseits auch manche der seit langem gemachten Beobachtungen, Vermutungen und Empfehlungen (Linseisen et al 2007, Boeing 2007, Bofetta et al 2010).
Beeinflusst Übergewicht das Prostatakrebsrisiko?
Zusammenhänge zwischen starkem Übergewicht (Fettleibigkeit) und Prostatakrebs sind in vielen Beobachtungsstudien dokumentiert. Es ist ziemlich eindeutig, dass übergewichtige Männer (gemessen mit dem BMI, dem Bauchumfang und der waist-hip-ratio) krebsgefäherdeter ssind. Ob Übergewicht jedoch selber für die höhere Aggressivität von Prostatakrebszellen tatsächlich eine Bedeutung hat, ist umstritten. Möglicherweise sind es nicht aggressivere Tumorzellen , sondern die veränderte Biologie des Gewebes in der Prostatadrüse, die aufnahmebereiter ist für die Invasion, die Ausdehnung und das Wachstum der Tumorzellen.
Gesichert ist, dass eine Prostatakarzinom-Erkrankung bei Übergewichtigen aggressiver verläuft als bei Normgewichtigen. Besonders gefährdet sind Männer mit „Bauchfett“.
Ein BMI von 24 – 29 ist bei älteren Männern (> 65 Jahre) nicht Besorgnis erregend, eher hingegen ein BMI > 30. Allerdings gibt es auch massiv Übergewichtige („happy obese“), die weder zu Diabetes und Herzerkrankungen noch zu Krebserkrankungen neigen. Ursächlich nimmt man bei ihnen eine bestimmte Enzymausstattung an (verminderte Hämoxygenase-1).
Ab wann ist man übergewichtig? Ab welchem Übergewicht ist man krebsgefährdet?
Übergewichtig ist man gemäß Definition der Weltgesundheitsorganisation (WHO), wenn der Body Mass- Index (Körpergewicht in Kilogramm dividiert durch Körpergröße in Metern hoch zwei) über 25 liegt. Ein 1,80 Meter großer Mann mit 85 kg ist demnach übergewichtig. Starkes Übergewicht – medizinisch auch Fettsucht oder Adipositas (Obesity) genannt – liegt vor, wenn der Body-Mass-Index (BMI) größer als 30 ist. 16 Prozent aller Männer sollen adipös sein.
Die Definition, ab welchem Übergewicht man krebsgefährdet ist, ist sehr umstritten. Man ist heute allgemein der Auffassung, dass mit zunehmendem Alter die Grenze von Normal- zu gefährlichem Übergewicht steigt.
Ein eindeutiges Prostatakrebsrisiko besteht nur bei starkem Übergewicht BMI>30); bei mittlerem Übergewicht (BMI zwischen 26 und 30) sind die Risiken weniger deutlich, wenn überhaupt.
Einteilung des Gewichts nach Body Mass Index (BMI
< 18,5 kg/m2= Untergewicht
18,5 kg/m2 bis 24,9 kg/m2= Normalgewicht
25,0 kg/m2 bis 29,9 kg/m2 = Übergewicht
>30,0 kg/m2 = Adipositas (starkes Übergewicht, Fettsucht)
30 – 35 kg/m2 = Adipositas Grad 1
35 – 40 kg/m2 = Adipositas Grad 2
> 40, 0 kg/m2= Adipositas Grad 3 (Adipositas permagna
Beispiel:
Ein Mann ist 1,76 m groß, 32 Jahre alt und 78 kg schwer. Sein Body Mass Index beträgt 78 kg / (1,76 m x 1,76 m) ≈ 25,18 kg/m² ⇒ minimales Übergewicht.
Das mit kg berechnete Übergewicht oder den BMI als alleinige Messgröße für ein Erkrankungsrisiko zu benutzen, ist nach neueren Erkenntnissen problematisch und überholt. Beim BMI wird nämlich nicht zwischen Fett und Muskeln unterschieden. Fett, besonders Bauchfett, hat jedoch bei der Risikoabschätzung von Krebs eine große Bedeutung. Würde man den BMI als alleinige Messgröße nehmen, so fielen Sportler mit viel Muskelmasse rein rechnerisch in die Kategorie „übergewichtig“ und wären somit krebsgefährdet, obwohl sie insgesamt wegen ihrer stärkeren körperlichen Aktivität ein geringeres Erkrankungsrisiko haben als Normalgewichtige.
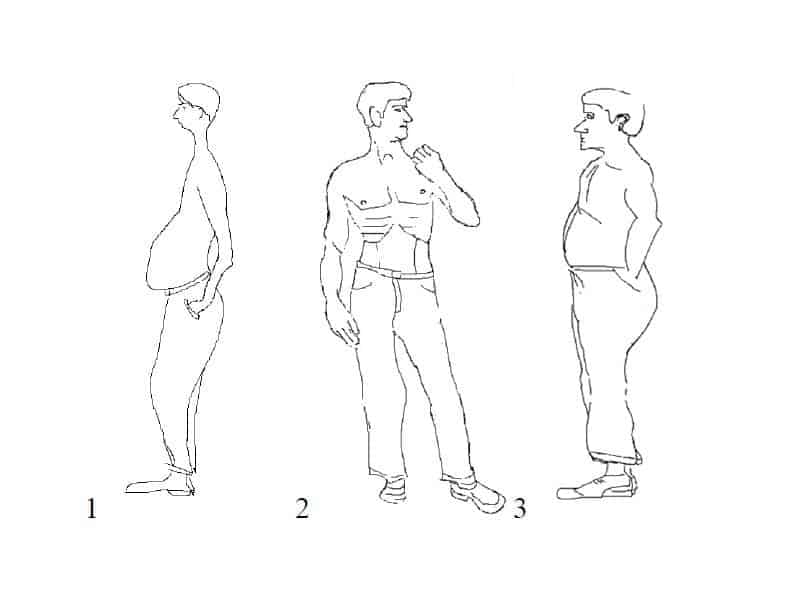
Besonders gefährdet sollen Männer mit „Bauchfett“ sein (Pischon et al 2008, Giovannucci et al 1997, Brown et al 2009). Bei ihnen verteilt sich das Fett nicht über den ganzen Körper, sondern konzentriert sich auf die Bauchregion (Abbildung). So haben Männer mit einem Taillenumfang von mehr als 120 Zentimeter ein erhöhtes Krebsrisiko. Ein „Apfelbauch“ (dünne Beine, dicker Bauch) ist mit einem größeren Erkrankungsrisiko assoziiert als ein „Birnenbauch“ (überschüssiges Fett vor allem an den Oberschenkeln). Viele Experten messen daher dem Taille-Hüft-Verhältnis (Waist-Hip-Ratio)eine hohe Bedeutung bei. Die Waist to Hip Ratio errechnet sich aus dem Quotienten aus dem Taillenumfang in Zentimetern und dem Hüftumfang in Zentimetern. Ein erhöhtes Risiko besteht bei Männern ab 92 cm.
Die drei Risikotypen 1: hohes Risiko: Mann mit Bauchfett (dünne Beine, dicker Bauch 2) geringes Risiko: Übergewichtiger Mann mit athletischem Körperbau, 3) normales Risiko: Normgewichtiger Mann mit generalisierter Fettverteilung
Das Unterhautfettgewebe dagegen gilt als weitgehend harmlos. So leben beispielsweise Sumo-Ringer trotz ihrer beeindruckenden Körpermasse mit einem völlig normalen, nicht erhöhten Risiko sowohl für Krebserkrankungen als auch Erkrankungen des Herz-Kreislauf-Systems oder Diabetes. Bei ihnen sind dank eines straffen Trainingsprogramms unter hochkalorischer Nahrungsaufnahme zwar die äußeren Körperschichten gut gepolstert, zwischen Leber und Milz aber findet sich so gut wie kein überflüssiges Fett.
Diese Tatsache erklärt möglicherweise auch, warum sich das Krebsrisiko übergewichtiger Menschen auch dann durch körperliche Aktivität verringern lässt, wenn sie dabei gar nicht abnehmen. Mangelnde körperliche Aktivität und Übergewicht scheinen in vielen Fällen weitgehend voneinander unabhängige Risikofaktoren zu sein.
Wie erklärt man sich die krebsfördernde Wirkung von starkem Übergewicht?
Es gibt hierfür mehrere Hypothesen. So soll es bei einer Adipositas zu einer tumorfördernden Biologie des Prostatagewebes kommen, so dass Krebszellen eher sich ausbreiten können. Auch sollen die Insulinresistenz und der assoziierte hohe Insulinspiegel – ein gemeinsamer Risikofaktor für Adipöse und Typ-2-Diabetiker- das Tumorwachstum sowie die Gefäßbildung stimulieren. Fettgewebe produziert Adipokine sowie Signallipide wie Eicosanoide, Phosphoinositide, Sphingolipide und Fettsäuren, die das Zellwachstum anregen. Eine Stimulation durch Testosteron ist sehr unwahrscheinlich, weil der Testosteronspiegel bei Übergewichtigen eher erniedrigt ist im Gegensatz zu den Östrogenen. Der niedrigere Androgenspiegel im Blut adipöser Männer könnte sich sogar krebsfördernd auswirken, da die hormonunabhängigen, und somit bösartigeren Krebszellen einen Selektionsvorteil hätten (Hayashi et al 2014).
Bei Adipösen bestehen im Übrigen häufig subakute chronische Entzündungen, die Gene oder Signalwege aktivieren oder unterdrücken.
Hypothesen für die Krebsförderung durch Übergewicht.
Fettgewebe produziert Adipokine sowie Signallipide wie Eicosanoide, Phosphoinositide, Sphingolipide und Fettsäuren, die das Zellwachstum anregen.Es kommt zu einer krebsfördernden MikroumgebungDie mit Übergewicht assoziierte Insulinresistenz führt zu einer kompensatorischen Vermehrung Insulin ähnlicher Substanzen (IgF1), die die Bösartigkeit von Krebsvorstufen fördern. . Übergewichtige sind meist auch wenig körperlich aktiv. Körperliche Inaktivität gilt allgemein als Krebsrisikofaktor.Bauchfett führt zu einer Fettleber, einem bedeutenden Krebsrisikofaktor. Übergewicht und speziell Bauchfett sind oft die Folge von kalorienreicher Ernährung, häufigem Fleischverzehr, reichlichem Alkoholkonsum und wenig Bewegung. Sie alle fördern die Entwicklung von Prostatakrebs.Sicherlich spielt die Vererbung eine Rolle. Bestimmte vererbbare Moleküle (z. B. die Hämoxygenase (HO-1) sollen mit über Gesundheit und Krankheit von stark Übergewichtigen entscheiden.
Fördert eine fleisch- und fettreiche Ernährung Prostatakrebs?
Von vielen Experten wird auf krebsfördernde Einflüsse einer fleisch- und fettreichen Ernährung (vor allem tierischer (gesättigter Fette) hingewiesen. Dafür gibt es sehr unterschiedliche Erklärungen (Giovanucci et al 1992 und 1993, Kristal et al 2010). So wird auf die wesentlich selteneren Prostatakrebserkrankungen in Japan und China hingewiesen, wo die Ernährung weniger gesättigte und mehr Fettsäuren enthält. Verglichen mit China essen Europäer 4 bis 11-mal so viel tierisches Eiweiß in Form von Fleisch, Wurst, Käse, Milch, Eier und Fisch. In Regionen, in denen westliche Ernährungsgewohnheiten übernommen wurden, shat sich auch die Häufigkeit und die Aggressivität von Prostatakarzinom-Erkrankungen erhöht. Einige Experten verweisen auf die häufig erhöhte IgF-1 (Insulin like Growth factor) Konzentration im Blut, die zu einem „oxydativem Stress“ durch freie Radikale führe und auf diesem Wege das Krebswachstum fördere.
Die Beobachtungen aus der EPIC Studie bestätigen grundsätzlich den Verdacht, dass ein hoher Fleischkonsum mit einem erhöhten Krebsrisiko. 300 bis 600 gr./wöchentlich sollen allerdings nicht schaden, wobei es auch unklar sei, ob alle Fleischsorten oder nur bestimmte Fleischsorten sich krebsgefährdend auswirken und ob nicht die Zubereitung des Fleisches (roh, medium, well done) bzw. die Art der Fleischverarbeitung für die Krebsgefährdung verantwortlich sind.
Führt ein hoher Konsum von Milch bzw. Milchprodukten zu einer erhöhten Gefährdung?
Ein hoher Verzehr an Milchprodukten soll die Wahrscheinlichkeit einer Prostatakarzinomerkrankung leicht erhöhen, hingegen nach Beobachtungen aus der EPICStudie das Risiko der Entwicklung eines Darmkrebses mindern (Gao et al 2005, Kristal et al 2010). Das Max Rubner Institut (MRI) meint, dass das Risiko wahrscheinlich nicht an dem in Milchprodukten enthaltenen Kalzium liege, sondern eher im Zusammenhang mit dem Fettgehalt stehe (Skinner et al 2009). Milch und Milchprodukte enthalten einen hohen Anteil an gesättigten Fettsäuren. Außerdem befinden sich in der Milch insulinähnliche Wachstumsfaktoren wie IgF-1.
Ein negativer Einfluss des Kalzium – Spiegels auf die Entwicklung von Prostatakarzinomen wird zwar allgemein verneint, jedoch vor einer zu hohen Kalziumaufnahme wegen der möglichen Nebenwirkungen auf Herz Kreislauf gewarnt. Kalzium ist wichtig für viele Stoffwechselvorgänge, jedoch kann sich zu viel Kalzium schädlich auswirken (Giovannucci et al 2006, Mitrou et al 2007, Halthur et al 2009, Williams et al 2012). Auf eine Nahrungsergänzung mit Kalzium und Folsäure sollten Männer sowohl wegen des lange in Verdacht stehendem Prostatakarzinom – Risiko, aber auch drohender Herz-Kreislauf-Probleme verzichten (Vollset et al 2013).
Ist ein Vitaminmangel für Prostatakrebs (mit)verantwortlich?
Vitaminmangelzustände haben nach den Beobachtungen in neueren Studien, so der EPIC Studie, eine wesentlich geringere Bedeutung als man früher annahm (Bofetta et al 2010).
Zwar haben Krebspatienten häufig einen niedrigeren Vitaminspiegel im Blut, der aber eher Folge als Ursache der Krebserkrankung ist. Viele Therapiestudien belegen, dass sich trotz laborchemisch feststellbarer Normalisierung eines zuvor erniedrigten Vitaminspiegels keinerlei positive Auswirkungen auf die Krebsentwicklung ergeben. Es bestätigt sich immer wieder, dass ein verbesserter Laborwert noch lange nicht bedeutet, dass es einem Patienten bessergeht!
Bestimmte Nahrungs- und Nahrungsergänzungsmittel, Enzyme, Mineralstoffe und Spurenelemente, die in der Vergangenheit sehr häufig zur Steigerung der Abwehrkräfte und zur Krebsverhinderung eingenommen wurden, gelten heute sogar als schädlich. Folsäure kann dazu führen, dass Darmpolypen schneller wachsen und bei genetischer Vorbelastung zu Darmkrebs führen. Vitamin E und Betacarotin erhöhen das Lungenkrebsrisiko bei Rauchern, die Einnahme von Vitamin E-Präparaten fördert möglicherweise die Entwicklung von Prostatakrebs (Tombal 2012).
Alarm löste 2007 die Beobachtung einer Studie des Nationalen Krebsforschungsinstituts der USA aus, in der es um Auswirkungen von Multivitaminpräparaten auf das Prostatakrebsrisiko ging (Lawson et al 2007). Teilnehmer der einen Studiengruppe hatten hoch dosierte Vitamine erhalten, die Teilnehmer der anderen Gruppe Placebo Präparate. Unterschiedliche Krebshäufigkeiten wurden zwar nicht beobachtet, jedoch waren die Krebserkrankungen in der „Vitamingruppe“ häufiger bösartig. Die Prostatatumore hatten sich wesentlich zahlreicher ins Gewebe ausgedehnt und Metastasen gebildet.
Vitamine und Mineralstoffe, die in Obst und Gemüse reichlich enthalten sind, haben hingegen noch niemandem geschadet, ja die meisten Ernährungsexperten erwarten nach wie vor ein niedrigeres Krebsrisiko, wenn bevorzugt Obst und Gemüse, und weniger Fleisch, gegessen wird.
Verursacht ein Vitamin- D- Mangel Krebs?
Besonders bei aggressiven Tumoren ist der Vitamin D-Spiegel häufig erniedrigt. Neuere Studien bezweifeln jedoch einen Einfluss auf die Krebsentwicklung (Zeeb und Greinert 2010), Hahne 2011) und halten einen Vitamin-D-Mangel eher für eine Folge und nicht Ursache der Krebserkrankung.
Können sich Vitamine und Spurenelemente auch krebsfördernd auswirken?
Es gibt Mutmaßungen, dass sich nach längerer Einnahme von Vitamin E und Selen das Prostatakarzinomrisiko erhöhen könnte. In der Select Studie (Klein et al 2011), in der ursprünglich eine Schutzwirkung von Vitamin E und Selen nachgewiesen werden sollte, stellte sich zur großen Überraschung das Gegenteil heraus. Männer, die täglich Vitamin E in handelsüblichen Dosierungen einnahmen, erkrankten tendenziell häufiger an Krebs, der darüber hinaus auch besonders bösartig war. Bei den Studienteilnehmern, die Selen erhalten hatten, kam es häufiger zu Diabetes und ebenfalls überdurchschnittlich häufig zu Krebs.
Die Beobachtung, dass Prostatakarzinom-Erkrankte häufig erniedrigte Zinkspiegel aufweisen und dass Zink sowohl das Zellwachstum als auch das Invasionspotential von Prostatakarzinomzellen unterdrückt, haben zu der Hypothese einer Schutzwirkung von Zink geführt. In der „Health Professionals Follow-Up Study“ stellte man jedoch fest, dass sich bei einer täglichen Zinkaufnahme von mehr als 100 mg das Prostatakarzinomrisiko eher erhöht. Hochdosiertes Zink fördert nachgewiesenermaßen die Entstehung von Prostatakrebs und anderen Tumoren des Urogenitaltraktes.
Ist Alkohol ein Risikofaktor?
Zwar gibt es viele Studien, die sich mit der Frage eines möglichen Zusammenhangs von Prostatakarzinomen und Alkohol befasst haben, jedoch gibt es keine wissenschaftlich überzeugende Studie, die einen eindeutigen Zusammenhang oder gar einen Schwellenwert nachgewiesen hätte.
Der Grund für die sehr unterschiedlichen Ergebnisse und Empfehlungen könnte die Abhängigkeit der Alkoholverträglichkeit von der ethnischen Zugehörigkeit, vom Geschlecht, vom Alter, vom Körpergewicht, vom allgemeinen Gesundheitszustand, Begleiterkrankungen und vielen anderen Faktoren sein.
Während die meisten Experten keinen Zusammenhang festzustellen glauben, gehen andere Autoren von einem erhöhten Risiko nur bei starkem Alkoholkonsum aus (50 g und mehr Alkohol täglich) (Kristal et 2010). Sie sagen, dass chronischer Alkoholkonsum zu einer Erhöhung einiger Hormonspiegel im Blut führe, so von Testosteron und Insulin, denen eine Wachstum fördernde Wirkung von Prostatakrebszellen nachgesagt wird. Dieser Vorstellung steht allerdings die Erfahrung gegenüber, dass diese Hormone bei einer alkoholbedingten Leberzirrhose eher erniedrigt und die Östrogene erhöht sind, weswegen eine Leberzirrhose das Krebswachstum eher hemmen müsste (Watters et al 2010).
Früher hatte man besonders den Bierkonsum für gefährlich gehalten. Heute führt man jedoch das erhöhte Krebsrisiko bei Biertrinkern auf deren häufiges Übergewicht zurück. Starkes Übergewicht soll ein Risikofaktor für Prostatakrebskranke sein. Bier ist sehr kalorienreich.
Wirkt sich häufiger Kaffeegenuss krebsfördernd aus?
Hierfür gibt es keinerlei Hinweise. Im Gegenteil, es gibt Beobachtungen, dass starke Kaffetrinker weniger häufig an Prostatakrebs versterben (Wilson et al 2011 und 2013). Die im Kaffee enthaltenden antioxydativen und antientzündlichen Substanzen sollen eine Schutzwirkung haben.
Ist „Fast food“ krebsfördernd?
„Fast food“ ist sehr kalorienreich und enthält viel Fett, gesättigte Fettsäuren, Zusatzstoffe, Zucker und Salz. Einige Experten halten das bei der Erhitzung von Pommes Frites entstehende Acrylamid für erbgutschädigend. Schon allein wegen der Förderung von Übergewicht ist Fast food ungesund.
Zudem ist Fast food wegen des hohen glykämischen Index nicht ratsam. Je höher der glykämische Index (GI) einer Ernährung, desto höher die Insulinausschüttung, umso stärker ist die Krebsförderung, meinen viele Experten! Der glykämische Index ist ein Maß für die Blutzucker steigernde Wirkung von Nahrungsmitteln. Er ist bei Süßigkeiten und bei fast food besonders hoch.
Haben Süßstoffe in Getränken einen Einfluss?
Lange Zeit wurde der Süßstoff Aspartam mit diversen Gesundheitsgefahren in Verbindung gebracht. Eine ausführliche Untersuchung der EU-Lebensmittelbehörde (Efsa) hat jedoch ergeben, dass der künstliche Süßstoff in den erlaubten Mengen für Verbraucher ungefährlich ist. Die empfohlene Tageshöchstdosis in der EU liegt bei 40 Milligramm pro kg Körpergewicht. Ein Kind mit 20 kg Körpergewicht könnte der Efsa zufolge täglich anderthalb Liter, mit Aspartam gesüßte Limonade trinken, ohne den Grenzwert zu erreichen.
Quelle und Buch-Tipp:
Prostatakrebs vermeiden (Personalisierte Krebsvorsorge und Früherkennung)
Hermann Delbrück ist Arzt für Hämatologie – Onkologie und Sozialmedizin sowie Rehabilitation und physikalische Therapie und Hochschullehrer für Innere Medizin und Sozialmedizin. Während seiner Laufbahn in der experimentellen, kurativen und vor allem rehabilitativen Onkologie veröffentlichte er mehrere Lehrbücher. Er ist der Herausgeber zahlreicher Ratgeber für Betroffene mit Krebs. Seit seiner Emeritierung 2007 befasst er sich vorrangig mit Fragen der Prävention von Krebs.